Ley de los gases ideales.
Esta ley establece el estado del gas ideal, el cual esta formado por partículas sin atracción o repulsión entre ellas, y cuyo choque es perfectamente elástico.
A temperatura constante, la presión de una masa fija de gas, es inversamente proporcional al volumen de este.

La temperatura usada en la ecuación, sería una temperatura absoluta, y esta a la vez es directamente proporcional a la presión y al volumen.
Ley de Avogadro.
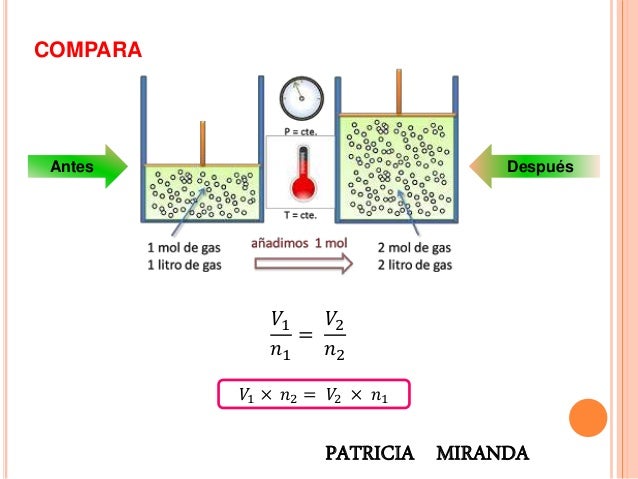
Esta ley relaciona la cantidad de gas con el volumen mismo a temperatura y presión constantes,
mientras más moles de gas tengamos, más volumen tendrá el gas.
La diferencia entre volumen y moles del gas es una constante, por lo que:
No hay comentarios:
Publicar un comentario